ABSTRACT
Obiettivo: l’insufficienza venosa cronica cerebrospinale (CCSVI) è un quadro vascolare caratterizzato da stenosi combinate delle principali vie del drenaggio venoso extracranico, che riguardano le
vene interne giugulari (IJV), e la vena azygos (AZY); ne deriva la formazione di circoli collaterali e insufficiente drenaggio venoso dimostrato da un maggiore tempo di transito (perfusionale) in studi
cerebrali MRI perfusionali. L’CCSVI è fortemente associata a sclerosi multipla (MS), una malattia neurodegenerativa considerata di origine autoimmune. Lo scopo di questo studio è di valutare la
sicurezza del trattamento endovascolare CCSVI e l’impatto sul decorso clinico della MS.
Metodi: Sono stati analizzati 65 pazienti tutti affetti da CCSVI e suddivisi in base al decorso clinico della MS: 35 con decorso a remissione ricorrente (RR), 20 di loro avevano un decorso progressivo secondario (SP), e 10 progressivo primario (PP), sottoposti ad angioplastica percutanea transluminale (PTA).
La durata di un follow-up medio è stata di 18 mesi. Le variabili considerate in base ai risultati vascolari sono: complicazioni postoperatorie, pressione venosa, percentuale di pervietà dei vasi nel follow-up. Variabili neurologiche considerate: funzionalità motoria e cognitiva (MSFC), di ricaduta della MS, frequenza
all’indagine MRI di lesioni MS attive positive in base alla maggiore acquisizione del gadiolino (Gad+, parametro misurato in cieco), questionario Qol MS (qualità di vita dei pazienti con sclerosi multipla).
Risultati: Dividiamo I risultati in due sezioni:A) Risultati sul versante vascolare: Il trattamento endovascolare del CCSVI è stato realizzato in regime di Day Surgery con un tasso di complicazioni irrilevante, minimo. La pressione venosa postoperatoria è risultata significativamente più bassa nel IJV come pure nell’ AZY (p<0.001). Il rischio di restenosi nell’IJV è risultato maggiore rispetto all’AZY (tasso di pervietà 53%, tasso dell’AZY 96%, rispettivamente. OR 16, 95% CI 3.5-72.5 p<0.0001).
B) Risultati sul versante neurologico: ll numero di pazienti senza recidive è passato dal 27% al 50% postoperativamente (p<0.001), e quello con lesioni evidenti alla RM Gad + dal 50% al 12% (p<0.0001); l’MSFC in un anno è migliorato considerevolmente in RR (p<0.008), C) ma non nelle forme PP o SP, infine la QoL fisica è migliorata in modo considerevole negli RR (p<0.01) e in pazienti con decorso clinico di tipo PP(p<0.03), con un trend positivo negli SP (p<0.08). La QoL mentale ha mostrato un consistente miglioramento negli RR. (p<0.003) e in PP (p<0.01) ma non nell’ SP.
Conclusione: Il PTA delle stenosi venose in pazienti CCSVI è utile, specialmente in pazienti con SM a decorso RR, in cui ha dimostrato di poter influenzare positivamente i parametri Qol e clinici dell’MS rispetto alla valutazione preoperatoria. Il dato obiettivo (in cieco) della riduzione delle lesioni attive alla RMN è superiore a quello ottenuto fin ora con qualunque altra terapia.
Le percentuali di restenosi sono risultate elevate nell’IJV ma molto meno frequenti nell’AZY, suggerendo quindi la necessità di migliorare le tecniche endovascolari nel primo settore venoso. Il risultato di questo studio pilota pretende attenzione e un successivo studio clinico randomizzato.
INTRODUZIONE
Il sangue lascia il cervello utilizzando la propulsione di ritorno della pressione arteriosa residua (vis a tergo), integrato da meccanismi anterogradi posturali e respiratori (vis a fronte)1,2. Questi ultimi consistono in un aumentato flusso venoso durante inspirazione, grazie ad una aumentata pressione toracica negativa che
determina l’aspirazione del sangue verso l’atrio destro. Inoltre, la posizione supina favorisce il flusso venoso cerebrale attraverso le vene giugulari interne (IJV); al contrario, in posizione ortostatica, il sangue viene ridiretto attraverso le vene vertebrali (VV), e la vena azygos (AZY), che diventano le principali vie di reflusso in questa posizione1,2
.
Le vene cerebro-spinali extracraniali formano un complesso sistema vascolare deficitario di valvole (Fig. 1) con l’eccezione dell’IJV. Sebbene la presenza di valvole nella posizione distale dell’IJV sia stata ampiamente descritta da anatomisti e patologi, la loro esistenza viene sottolineata nella letteratura medica. Nel 93%
di studi post-mortem furono riscontrate valvole nella porzione distale delle vene giugulari interne.
L’ultrasonografia ha facilmente dimostrato tracce di valvole nell’87% di pazienti; tutti osservati nella porzione distale dell’IJV3
.
L’insufficienza venosa cerebrospinale cronica (CCSVI) è un quadro vascolare recentemente esaminato e caratterizzato da stenosi multiple delle principali vie del drenaggio venoso extracraniale, specialmente nell’IJV e nell’AZY. Ne deriva l’apertura di circoli collaterali, chiaramente dimostrati per mezzo di venografia selettiva4
.
Studi flebo grafici dei sistemi IJV e AZY hanno dimostrato che le stenosi venose erano molto probabilmente malformazioni venose di tipo tronculare5 . È stato riscontrato che la CCSVI è fortemente
collegata alla sclerosi multipla (MS), una malattia neurodegenerativa invalidante e demielinizzante considerata di origine autoimmune, ma non era mai stata prima d’ora collegata a varie altre condizioni neurologiche, come pure in controlli sani 4,6
.
Le frecce si riferiscono alla direzione del flusso venoso fisiologico direzione. Il tasso percentuale
indica la posizione e la prevalenza di stenosi venose osservate nel quadro dell’insufficienza
venosa cronica cerebro-spinale. AZY, vena azygos; IVC, vena cava inferiore; L REN, a sinistra della
vena renale, LV, vene lombari; PterPlex, plesso pterigoideo, uno dei principali garanti del deflusso
venoso intra-extracranico; SVC, vena cava superiore; VPlex, plesso vertebrale. VV, la vena vertebrale
Nella CCSVI, come si è visto, vengono attivati circoli collaterali.
Essi by-passano le vene ostruite e quindi riducono la resistenza al drenaggio, evitando l’ipertensione intracranica. Tuttavia, il tempo del flusso venoso è maggiore rispetto al normale, provocando un
insufficiente drenaggio venoso, come confermato dal tempo di transito misurato mediante studi di perfusione con RM; anche nella sostanza bianca apparentemente normale.
In conclusione, la venografia, la RM e gli studi post-mortem hanno dimostrato una corrispondenza topografica tra le placche MS ed il sistema venoso cerebrale.
L’insufficienza venosa cronica cerebro spinale può essere diagnosticata non-invasivamente attraverso un eco-color-doppler (ECD) combinato trans craniale e extracranicale atto a misurare cinque parametri indicativi del CCSVI :
1) Presenza di reflusso nelle vene giugulari interne e/o nelle
vene vertebrali con il capo in qualsiasi posizione;
2) Presenza di reflusso nelle vene cerebrali profonde;
3) Presenza di stenosi evidenziabili mediante l’utilizza di sonda
Doppler ad elevata risoluzione
4) Flusso Doppler non rilevabile nelle vene giugulari interne o
nelle vene vertebrali
5) Perdita del fisiologico controllo posturale sul deflusso venoso
dei vasi cerebrali, espressa attraverso una riduzione
dell’area di sezione vascolare (∆csa negativo).
Abbiamo precedentemente descritto in letteratura che la diagnosi del CCSVI deve soddisfare almeno 2 dei 5 parametri ECD dell’CCSVI4,6
.
L’osservazione di ≥2 criteri nello stesso soggetto non si è mai verificata nei controlli, ma ha coinciso perfettamente con la diagnosi di un MS clinicamente definita in una valutazione di pazienti e controlli omogenei per età e sesso.
La SM viene classificata sulla base di tre principali decorsi clinici della malattia:
1) Forma recidivante remittente (RR), con cui spesso esordisce la malattia stessa ed è caratterizzata da acute esacerbazioni seguite da recupero completo inizialmente e poi sfortunatamente solo parziale nel tempo di un mese;
2) Forma secondaria progressiva (SP) caratterizzata da un progressivo deterioramento delle funzioni neurologiche, generalmente insorge dopo diversi anni dalla diagnosi di SM, ed è preceduta dalla forma RR;
3) Forma Primaria Progressiva (PP) caratterizzata dall’assenza di attacchi acuti, ma da un decorso clinico progressivo a partire dall’esordio.15,16
Il comitato etico ospedaliero, ha autorizzato l’indagine flebografica nei pazienti che nel febbraio 2007 erano stati sottoposti a screening con ECD ed erano risultati positivi per CCSVI, consentendo contemporaneamente il trattamento endovascolare di stenosi venose extracraniche qualora le lesioni fossero state dimostrate radiologicamente.
Abbiamo quindi concentrato la nostra attenzione su 65 pazienti consecutivi, affetti da sclerosi multipla, il cui decorso clinico, l’emodinamica e le caratteristiche venografiche sono state precedentemente descritte in altre pubblicazioni4
.
L'obiettivo di questo studio è stato quello di valutare la sicurezza, la fattibilità, e l’esito vascolare dell’angioplastica percutanea transluminale nel trattamento di lesioni ostruttive dei vasi intra ed
extracranici; come pure l'influenza del risultato sulla clinica, sul decorso e sui parametri RM valutati in cieco dei pazienti con un follow up medio di 18 mesi
PAZIENTI E METODI
Abbiamo selezionato 65 consecutivi pazienti affetti da SM clinicamente definita (CDMS), diagnosticati come da criteri McDonald (appendice)16. Nella loro selezione abbiamo adottato i seguenti criteri:
Criteri di inclusione
- Età 18-65 anni
- Tasso di invalidità (EDSS) oscillante da 0 a 6.5 (appendice)17
- Diagnosi di MS come da criteri McDonald riveduti
(appendice)16
- In cura con trattamenti approvati
- Dimostrazione di ≥2 parametri ultra-sonografici, sopra
elencati, di flusso extracraniale cerebrale venoso sospetto4,6;
- Normale funzionalità renale
Criteri di esclusione
- Recidiva, progressione della malattia e trattamento steroideo nei 30 giorni precedenti lo studio (tutte le condizioni modificano significativamente i parametri clinici, rendendo inattendibile qualunque valutazione postoperatoria)
- Pre-esistenti patologie mediche associate con patologie cerebrali (altri disordini neurodegenerativi, insufficienza cerebrovascolare, storia conclamata di abuso d’alcol, ecc.)
- Funzionalità renale anomala
- Rifiuto di sottoporsi al trattamento endovascolare
STUDIO FLEBOGRAFICO DEL DRENAGGIO VENOSO CEREBROSPINALE
I pazienti selezionati sono stati sottoposti ad un test di screening non-invasivo e molto accurato per verificare la presenza di CCSVI, basato su un protocollo ECD di indagine precedentemente descritto4,6
.
Il ritorno cerebrospinale venoso è stato esaminato per mezzo di ECD nei pazienti MS posizionati su un letto reclinabile fra gli O° e 90°. L’indagine si è focalizzata sulla localizzazione dei cinque parametri Doppler emodinamici sopra specificati (appendice).
Venografia selettiva
I pazienti si sono successivamente sottoposti a flebografia selettiva delle vene lombari, della vena renale sinistra, AZY, e IJV per mezzo di caterizzazione dell’asse venoso femorale sinistro iliaco4
. Il PTA è stato eseguito esclusivamente ai livelli dell’AZY e
IJV quando sono state rilevate stenosi significative.
Abbiamo ritenuto significativa una stenosi qualora presentasse una riduzione del lume venoso maggiore del 50%4,18,19
.
Per quanto riguarda la morfologia abbiamo considerato le seguenti malformazioni:
- Annulus: si riferisce alla presenza di una significativa stenosi circolare della parete venosa.
- Setti endoluminali / valvola anomala: si riferisce ad un anomalo apparato della valvola che da origine a significativi ostacoli del flusso al livello della giunzione dell’IJV con il tronco brachio-cefalico (anonimo).
- Ipoplasia: si riferisce alla presenza di lunghi segmenti venosi sottosviluppati e di calibro insignificante.
- Torsione: si riferisce alla presenza di severe stenosi in conseguenza di un segmento venoso attorcigliato attorno al proprio asse.
- Ostruzione membranosa: si riferisce alla presenza di una membrana anomala che occlude quasi completamente una vena.
- Agenesia: si riferisce alla completa assenza anatomica di un segmento venoso.
PTA della vena Azygos e delle vene giugulari interne Per realizzare questa procedura, si è utilizzato un catetere angiografico (5 Fr Head hunter, lungo 90 cm, Terumo Europe, Leuven Belgio) introdotto mediante un accesso femorale che naviga sotto guida radiologica dalla vena cava inferiore alla
superiore misurando la pressione venosa con un manometro collegato al catetere.
La cateterizzazione selettiva viene successivamente eseguita a livello della vena Azygos introducendolo per pochi millimetri per poter osservare qualsiasi possibile riflusso nella vena verso il basso.
Con l’ausilio di una guida idrofila (diametro 0.035-inch Radiofocus Guide Wire M, Terumo Europe, Leuven Belgium), il catetere è stato collocato dentro la vena Azygos fino alla confluenza con la
vena emi-azygos misurandone in questa sede la pressione venosa.
A questo punto si è eseguita una flebografia digitale selettiva sottrattiva della vena azygos con una proiezione obliqua dx posteriore (15°-25°) e mezzo di contrasto (IOMERON 300 mg/ml, Bracco s.p.a. Italia) velocità (3 ml/s) e quantità (10 ml) con lo scopo di rispettare il normale flusso antegrado della vena e per
localizzare qualunque riflusso o stenosi a livello dell’arco dell’AZY.
Uno studio morfologico più esauriente dell’AZY, cioè retrogrado, può essere eseguito con maggiori flussi (8 ml/s) e quantità (30 ml).
In questo modo è possibile ottenere una completa opacizzazione del sistema di origine delle vene Azygos ed emi-azygos, fino alle vene lombari ascendenti.
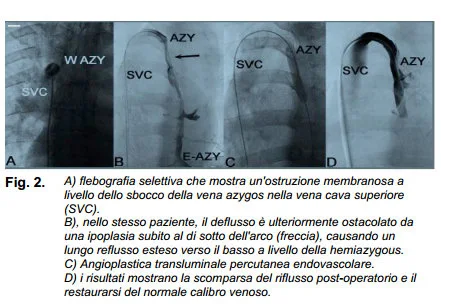
La presenza di anomalie ostruttive anatomiche come l’ostruzione membranosa, annulus, o torsione ha richiesto correzione endovascolare (fig. 1 e 2). Come prima procedura, abbiamo sempre eseguito la PTA
(angioplastica percutanea transluminale), utilizzando cateteri a palloncino di tipo compliante per la loro maggiore flessibilità che permette l’inserimento nell’arco ristretto dell’AZY. I palloncini (Opta Pro, Cordis Europa, Roden Netherland) che sono 8-10 mm di diametro e 2-4-6 cm di lunghezza sono stati utilizzati e gonfiati ad una pressione massima di 6 atmosfere.
La gonfiatura è stata mantenuta per 30-60 secondi e ripetuta varie volte. Al termine del procedimento terapeutico, sono state ripetute le misurazioni postoperatorie di pressione venosa e ripetuta la
flebografia selettiva dell’AZY e/o dell’IJV per poter documentare il risultato immediato del trattamento (Fig. 2).
Lo stesso catetere Head hunter utilizzato per l’AZY è stato poi reinserito per la flebografia selettiva di ambedue le vene giugulari interne, utilizzando la guida idrofila per passare attraverso il tratto
di IJV distale stenotico. Poi abbiamo eseguito una flebografia IJV (flow 3 ml/s, quantity 10 ml) in proiezione AP, completata con una proiezione obliqua, per poter localizzare la presenza di stenosi o
altre patologie più specifiche, come compressione ossea e malformazione delle valvole.
Anche nell’asse giugulare il primo tentativo per la dilatazione endovascolare dei tratti stenotici è stato sempre realizzato utilizzando palloncini complianti (Opta Pro, Cordis Europa, Roden Netherlands), con un diametro da 10 a 12 mm e una lunghezza di 4 mm, con una pressione di dilatazione di 6 atm. Un palloncino ad
alta pressione (Blue Max, Boston Scientific/MediTech, USA), 10x2 mm, 18-20 atm è stato impiegato successivamente in caso di annulus se il risultato ottenuto la prima volta è stato ritenuto insoddisfacente da parte degli operatori.
MISURE DI OUTCOME
Descriviamo le misure di outcome vascolare separatamente da quelle neurologiche associate aSclerosi Multipla, indipendentemente verificate dal ns team neurologico.
Misurazione esito vascolare (Vascular Outcome Measure) Abbiamo accertato quanto segue:
1) La pressione venosa espressa in cm/H2O misurata prima e dopo intervento tramite un manometro nella vena cava superiore, nell’AZY, ed in ambedue le vene giugulari int;
2) Il decorso postoperatorio e la percentuale di complicazioni.
In particolare, valutato la tolleranza dei pazienti alla procedura che misura il dolore come indicato dalla Visual
Analogue Scale (VAS)20 , trombosi postoperatoria; sanguinamento maggiore e minore; ed effetti avversi al mezzo di contrasto;
3) Tasso di pervietà utilizzando un monitoraggio ECD a 1,3,6,12,18 mesi, valutando gli stessi parametri preoperatori della CCSVI. Al termine del follow up di 18 mesi i pazienti
con restenosi sospette ECD sono stati sottoposti a venografia, come pure ad un eventuale secondo trattamento di PTA se necessario4,6 .Esito neurologico (Neurological outcome)
Il risultato neurologico è stato valutato dal team di neurologi (non in cieco) i quali hanno seguito il decorso clinico della Sclerosi Multipla.
Le misure sull’esito sono quelle di solito utilizzate in test clinici che esaminano il trattamento della SM:
1. Gravità della malattia. Qualunque trattamento sulla SMdovrebbe essere valutato mediante il test (MSFC)21,22, invece che il più largamente usato ma non sufficientemente dettagliato score di invalidità (EDSS)17 .
L’MSFC fornisce l’indice comprensivo Z per valutare la mobilità delle estremità superiori ed inferiori come pure la funzione cognitiva (appendice). Lo stesso medico ha eseguito l’accertamento MSFC preoperatorio e
postoperatorio sempre alla stessa ora ed allo stesso luogo e nelle medesime condizioni.
2. Recidiva in pazienti con decorso “RR”. Questo parametro clinico viene espresso dalla percentuale di pazienti che non hanno avuto ricadute in un anno e dal tasso annuo di recidive contro quello riportato durante i due anni precedenti il PTA23,25
. Questa valutazione è stata eseguita confrontando gli accessi per recidiva nel corso di tre anni e
mezzo (dato oggettivo) ambulatoriali in DH o ricovero ordinario.
3. QoL, utilizzando un questionario validato di 54 voci e rivolto a pazienti SM, suddiviso in 2 parti per valutare rispettivamente lo stato sia fisico che mentale26
Analisi statistica
I dati dei pazienti sono espressi come media e deviazione standard. Le differenze nella pressione venosa pre e postoperatoria sono state analizzate per mezzo del Mann-Witney test (a due code). Le differenze nella QoL e nel MSFC sono stateanalizzate con l’analisi one-way ANOVA. Le differenze nel tasso di
recidive annue e nella percentuale di pazienti con assenza di recidive come pure per le lesioni Gad+, sono state analizzate per mezzo del test exact Fisher a due code. Per ultimo, sono state
eseguite analisi sulle stenosi ricorrenti nell’AZY e nell’IJV mediante curva di sopravvivenza attuariale con stima Kaplan Mayer. Il valore P <0.05 è stato giudicato essere significativo per tutti questi test.
RISULTATI
Popolazione di pazienti In tavola II viene illustrata la popolazione di pazienti e lo stato di
disabilità in base alla MSFC e al EDSS.
Fattibilità e sicurezza della procedura
Tutte le procedure sono state eseguite in Day Surgery e mediante anestesia locale. La procedura è stata ben tollerata con una media di VAS 3.4±0.3. Nessuna complicazione operatoria o post operatoria è stata segnalata, come rottura dei vasi, trombosi, o effetti collaterali ai mezzi di contrasto.
Occasionalmente si sono verificate piccole emorragie con ematomi presso i punti di ingresso vascolari. Sei pazienti hanno riferito cefalea transitoria post-intervento, e spontaneamente risoltosi.
L’osservazione post-procedurale è durata una media di 4 ore e i pazienti dimessi con medicazione compressiva all’inguine sx, il miglior punto di accesso vascolare.
Una dose preventiva di eparina a basso peso molecolare (LMWH) è stata somministrata per le successive tre settimane in tutti i casi27
.Venografia selettiva: Localizzazione e morfologia di malformazioni venose stenosanti rilevate.
In pazienti con SM, le stenosi venose nelle principali vie di flusso cerebrospinale non sono mai state rilevate essere isolate, Invece,esse sono risultate essere combinate nell’IJV e AZY e nei sistemi
lombari, definendo 4 principali modelli di distribuzione4
:
Modello tipo A (30%) caratterizzato da stenosi significative sia dell’Azygos prossimale, oppure di uno dei due tronchi IJV, con la vena giugulare int controlaterale di aspetto compensatorio che
appare con una vasta area a sezione trasversale. Questo quadro è stato rilevato in 10/35 pazienti a decorso RR, ed in 5/20 a decorso SP, rispettivamente e mai in pazienti a decorso PP.
Modello tipo B (38%) caratterizzato da stenosi significative diambedue gli assi IJV e della vena azygos prossimale; osservato in 19/35 pazienti RR, in 9/20 SP, ed in 1/10 pazienti PP rispettivamente.
Modello tipo C (14%) caratterizzato da stenosi bilaterali in ambedue i tronchi giugulari con Azygos di aspetto normale; osservato in 4/35 pazienti a decorso RR e in 5/20 pazienti a decorso SP, mai nei pazienti a decorso PP.
Modello tipo D (18%) caratterizzato da stenosi a piu’ livelli dell’Azygos e delle vene lombari. L’associazione con la IJV è stata osservata in circa il 50% dei casi, causando un’ostruzione ulteriore in questi pazienti. È stata osservata in 2/35 pazienti RR, ed in 1/20 SP, rispettivamente e in ben 9/10 dei pazienti PP.
La tabella III riporta la morfologia flebografica delle malformazioni osservate nei diversi tronchi venosi. Le ostruzioni membranose dell’outlet dell’AZY nella SVC sono risultate essere le presentazioni più frequenti in tale segmento (Fig. 2).
L’attorcigliamento nell’AZY è stato osservato in 12/65 casi (Fig. 3).
Per quanto concerne le IJV, la maggior parte delle stenosi sono risultate essere morfologicamente correlate alla presenza di annulus (Fig. 4). Il setto è stata la seconda presentazione più frequente, che include anche le malformazioni dei lembi della valvola giugulare (Fig. 6). Infatti, le cuspidi della valvola erano
qualche volta fisse e immobili, oppure invertite rispetto alla posizione del cuore (Fig. 6). Infatti, le vene lombari sono state raramente colpite e la malformazione più frequentemente
osservata è risultata essere l’agenesia.
Outcome vascolare
Pressione venosa: i valori di pressione nei segmenti che presentano stenosi erano più elevati ma non significativamente diversi da quelli che presentavano venogrammi normali. Di contro,
i valori di pressione postoperatori sono risultati molto più bassi in tutti i segmenti (p<0.0001). La figura 5 riporta i valori di pressione pre e post operatori misurati in cm/H2O nell’AZY e in tutti e due gli
assi venosi IJV.
La percentuale di pervietà è risultata essere strettamente dipendente dal tipo e dalla localizzazione delle malformazioni venose del tronco sopra descritte. Nell’AZY la PTA ha dato il
miglior risultato con un tasso cumulativo di pervietà del 96%, incluse le procedure per le ostruzioni membranose, attorcigliamento e ipoplasia (Fig. 7).
In particolare, le ostruzioni membranose hanno mostrato un tasso di pervietà del 100% (Fig. 1). L’attorcigliamento è stato osservato in 12/65 casi, e in un caso non si è risolto con successo per mezzo
di un semplice PTA, ma ha richiesto il collocamento di uno stentmetallico auto-espandibile di diametro di 12 mm (fig. 3). In un secondo caso trattato con semplice PTA si è evidenziata una
recidiva dell’attorcigliamento durante il follow-up. L’ipoplasia ha risposto efficacemente in 5/6 casi (Fig. 2).
Il problema principale è stata la pervietà primaria a seguito della tecnica PTA al livello dell’IJV. La curva di sopravvivenza in fig. 7 mostra la distribuzione cumulativa delle restenosi a 18 mesi (47%)
con una percentuale di pervietà complessiva del 53%. La curva indica il picco di occorrenza di restenosi a circa 8-9 mesi dopo il procedimento chirurgico. Il rischio di restenosi nell’IJV è più alto di
16 volte rispetto quello dell’AZY dopo PTA (OR 16, 95% CI 3.5- 72.5 p<0.0001).
La venografia eseguita al termine del follow-up di 18 mesi in pazienti con sospette restenosi ECD ha confermato nel 100% dei casi il quadro di re-stenosi sospettato con ECD.
Outcome neurologico
1. Intensità (gravità) della patologia.
In pazienti RR, l’MSFC ha mostrato un miglioramento significativo a 18 mesi, come chiaramente mostrato nella tavola IV (p<0.008). Al contrario, l’MSFC ha mostrato un miglioramento significativo sebbene limitato dopo i primi 6 mesi in ambedue i corsi clinici PP e SP, ma a 18 mesi non ha evidenziato alcun miglioramento rispetto ai valori di base.
(tav. V).
2. Recidiva in pazienti RR:
La percentuale di pazienti che non hanno riportato recidive nell’anno precedente il trattamento endovascolare era stato solo del 27%, significativamente diversa dal 50% dimostrato nel follow-up post operatorio (tav. IV).Infine, tutti i pazienti RR con pervietà post procedurale dell’IJV e AZY non hanno
mai avuto recidive nel follow-up.
Questo significa che la riaccensione clinica della malattia si è avuta solo nel 50% dei pazienti con re stenosi dell’azygos o giugulare ma mai nei pazienti con normalizzazione persistente del drenaggio venoso cerebrale.
3. Misura di outcome in cieco mediante la risonanza magnetica perfusionale:
La percentuale di pazienti con lesioni positive al test con gadolino (active gadolium enhanced lesions) all’MRI si è considerevolmente abbassata dal 50% al 12% p<0.0001 (Tav. IV).
4. QoL: in pazienti RR il QoL sia fisico che mentale è significativamente migliorato, rispettivamente p<0.00
p<0.003, 8tav. IV). In ambedue i gruppi di pazienti PP e SP, il QoL ha mostrato un limitato miglioramento mentale e fisico dopo i primi 6 mesi, ma non a 18 mesi (tav.V).
DISCUSSIONE
L’insufficienza venosa cronica (IVC) e la CCSVI associata alla sclerosi multipla hanno molte somiglianze, basti analizzare i meccanismi molecolari e fisiologici implicati nello sviluppo delle
malattie iron-mediated(ferro mediata).
Nell’IVC la catena è scatenata da un’alterazione dell’emodinamica venosa con una conseguente microcircolazione sovraccaricata, causando lo stravaso dell’eritrocita che diventa la fonte primaria di
deposito di ferro.
Nella CCSVI associata alla sclerosi multipla, l’ostruzione venosa extracranica presumibilmente sovraccarica la microcircolazione cerebrale dato che l’istologia conferma lo stravaso dell’eritrocita
nelle placche cerebrali della sclerosi multipla proprio a livello perivenulare28,29
.
Il CCSVI è un quadro vascolare complesso caratterizzato da
lesioni venose ostruttive che interessano le principali vie di flussovenoso extracraniche cerebrali. La venografia selettiva ci ha permesso di eseguire un primo trattamento della lesione venosa
localizzata al momento della valutazione diagnostica per mezzo di angioplastica con palloncino in un gruppo di 65 pazienti consecutivi affetti da CCSVI4
. Abbiamo seguito i pazienti per 18 mesi, monitorando il risultato vascolare come pure quello
neurologico della sclerosi multipla associata.
La principale scoperta del nostro studio è la dimostrazione che il trattamento endovascolare della CCSVI per mezzo della sola PTA è fattibile e sicuro. La procedura è ben tollerata e provoca una
percentuale trascurabile di complicazioni minori. La misura della pressione venosa è un fattore chiave nel nostro studio. I valori di pressione registrati in posizione supina in segmenti che evidenziano stenosi erano più elevati ma non significativamente diversi da quelli registrati in segmenti con normale venogramma. Questo risultato non è già sorprendente. Tutti i pazienti hanno evidenziato stenosi, sebbene diversamente
posizionate, in un albero venoso liberamente comunicante. Presumibilmente, questo influenza le rilevazioni nei segmenti venosi che non presentano stenosi. In contrasto, la pressione nell’AZY e nell’IJV era risultata precedentemente significativamente più elevate di quella misurata in soggetti sani al controllo, testimoniando quindi l’importanza emodinamica dell’ostruzione venosa4
. Nel presente studio, la PTA ha dimostrato una significativa diminuzione della pressione venosa in tutti i
segmenti trattati (fig. 5), correggendo immediatamente uno dei più ovvii parametri emodinamici. Le nostre scoperte sono conformi ad un ruolo di ipertensione venosa nella complessa patogenesi della SM, fino ad ora solo ipotizzata30,31
.La pressione venosa aumentata può stirare le pareti venosa a livello venulare in modo sufficiente da separare le strette giunturetra le cellule endoteliali che formano la barriera emato-encefalica32
.
I colloidi, le macromolecole l’eritrocita potrebbero quindi passare attraverso le membrane inducendo il processo infiammatorio28,29. Il marker istologico di ipertensione venosa nell’ insufficienza venosa
cronica degli arti inferiori, le cosiddette “cuffie di fibrina”, è stato altresì dimostrato nelle vene all’ interno delle placche della sclerosi multipla.
Inoltre, come precedentemente detto, i quattro modelli di ostruzione venosa sono diversamente distribuiti tra le categorie dei pazienti con sclerosi multipla in base al decorso clinico della malattia. L’83% dei pazienti con decorso RR e il 92% dei pazienti a decorso SP tra i modelli A, B, C della CCSVI laddove il decorso
PP e collegato invece al modello D nel 90% dei casi. Quindi nel decorso PP della SM (caratterizzato da una topografia delle placche nel midollo) le stenosi sono state riscontrate prevalentemente nelle vene che drenano il midollo spinale4
.
Questa scoperta suggerisce che il tipo emodinamico di CCSVI influenza la distribuzione delle lesioni e il decorso clinico della SM contribuendo a spiegare inoltre il diverso risultato postoperatorio nei tre sottogruppi di pazienti con SM.
L’Outcome postoperatorio a lungo termine è dipeso dal segmento e dalla morfologia della malformazione venosa.
Il distretto della vena Azygos è risultato interessato nell’86% dei casi e tra questi la malformazione vascolare “ostruzione membranosa” a livello della giunzione con la vena cava superiore era la più frequente.Meno frequente è risultato l’attorcigliamento e ancor meno il setto e l’ipoplasia, come mostrato in tabella III.
In questi casi, l’eco-color Doppler preoperatorio aveva evidenziato un riflusso e/o un blocco del flusso nelle vene vertebrali sempre confermato dalla venografia che ci ha aiutato a documentare la
morfologia dell’ostruzione dell’Azygos, come anche la presenza di riflusso direzionato verso il basso e verso il midollo (Fig. 2)4
.
L’ostruzione membranosa dell’outlet è stata riscontrata nel 50% dei casi e il nostro studio ha dimostrato un efficace trattamento per mezzo di una semplice PTA, seguita da una percentuale di
pervietà a 18 mesi del 100%.
Morfologicamente, le ostruzioni membranose, assomigliano all’ostruzione membranosa della vena cava inferiore descritta nel caso della sdr di Budd-Chiari, ed i nostri risultati sembrano essere
compatibili con la percentuale di successo riportata e seguendo la PTA a questo livello18,19,34
.
Inoltre, simili stenosi venose, qualche volta complicate da successive trombosi venose, sono state anch’esse descritte e trattate con successo nella vena cava inferiore e nelle vene iliache19
.
Per quanto attiene alla loro origine, quest’area è considerata essere incline ad anomalie evolutive congenite o dello sviluppo dei vasi quali l’ostruzione membranosa e la stenosi.
Alcune parti della rete formativa venosa vanno incontro ad involuzione o residuano come rudimenti embrionali; altre parti sono riconoscibili nell’adulto come strutture definite, come la vena
Azygos e la vena emi-azygos, le vene toracolombari19 Abbiamo bisogno di ulteriori studi per poter definitivamente concludere se le malformazioni appena trattate possano essere
considerate di origine congenita o evolutiva. Se tale ipotesi dovesse essere confermata non possiamo
considerare la CCSVI e la SM come una semplice e causale associazione di patologie ma piuttosto come un potenziale fattore scatenante per lo sviluppo della Sclerosi Multipla.
L’attorcigliamento della vena Azygos è una malformazione venosa che non è mai stata descritta prima d’ora.
Ia PTA è stata efficace anche nel correggere la condizione di twisting dell’Azygos in 11 casi su 12. Solo in un caso per ottenere la rettilineizzazione del Twisting è stato necessaria l’inserzione di
uno stent (Fig. 3).
Per quanto attiene ai rimanenti 11 casi, uno di questi è andato incontro a recidiva del twisting dopo 6 mesi.
La percentuale di pervietà è stata altresì soddisfacente per il trattamento della PTA dell’ipoplasia della vena Azygos in 5 casi su 6, stabilendo una percentuale di pervietà cumulativa del 96% a 18 mesi (Fig. 7).
In 12 casi, il sistema venoso dell’Azygos ha mostrato stenosi in diversi punti, oltre che aspetti di agenesia dei plessi lombari (18%).
Si deve notare che la presentazione di tali malformazioni è stata ritenuta associata in modo significativo con il decorso PP della sclerosi multipla, le cui placche distribuite nel midollo spinale4
Ovviamente l’agenesia non può essere trattata con PTA e ciò probabilmente spiega i risultati peggiori ottenuti in questo gruppi di pazienti rispetto a quelli con decorso RR.
I risultati PTA in termini di pervietà primaria a livello della vena giugulare interna sono stati molto meno positivi. Nel senso che levene giugulari interne hanno riportato stenosi unilaterali o bilaterali
in 59 casi su 65 ( 91%). Le stenosi sono state causate per lo più da malformazioni del tipo “ annulus” ( fig 3), seguite da quelle tipo setto/ valvola (fig 6).
Le restenosi si sono verificate nel 47% dei casi in tutto. Le curve di sopravvivenza cumulative dimostrano che tali esiti negativi si sono verificati con maggiore frequenza negli 8-9 mesi successivi alla
procedura iniziale.
L’alternativa logica sarebbe stata l’introduzione di uno stent34; tuttavia ci siamo astenuti dall’adottare questa tecnica per l’assenza sul mercato di strumenti appropriati di opportune dimensioni.
Adattare stent già esistenti per la patologia arteriosa a livello della Vena giugulare int avrebbe aumentato il rischio di migrazione polmonare, di spostamento, influenzando quindi il deflusso venoso
dall’arto superiore. Inoltre non abbiamo dati sulla interazione biologica tra gli stent metallici e le vene nel corso degli anni; gli stent infatti potrebbero essere inglobati o fratturati e questo in
individui giovani potrebbe avere conseguenze disastrose.
Stiamo attualmente considerando la pervietà secondaria nello stesso gruppo di pazienti dove abbiamo eseguito, alla fine del follow-up, un secondo trattamento utilizzando un palloncino ad alta
pressione (20 atm).
Un'altra opzione possibile potrebbe essere quella di un opensurgery specialmente in pazienti che ottenuto benefici clinici, evidenti anche alla RM perfusionale dopo PTA, e che successivamente siamo andati incontro a peggioramento e/o ricaduta con concomitanti con l’evento restenosi.
L’ultimo aspetto, tra l’altro molto affascinante, di questo studio è la favorevole risposta neurologica nel paziente con Sclerosi Multipla.
Ciò è stato piuttosto evidente nei pazienti a decorso RR, in questo gruppo si è assistito ad un significativo e netto miglioramento delle funzioni cognitivo-motorie della patologia, con un miglioramento
parallelo anche della QoL.
La percentuale di pazienti che non hanno mostrato recidive è aumentata significativamente, d’altra parte non è stato cosi per la percentuale di recidive annue (tav IV).
È di grande interesse e dovrebbe essere sottolineato il fatto che non sono state rilevate ricadute in pazienti con una soddisfacente inversione della condizione di CCSVI , in termini di pervietà stabile
sia nella vena giugulare interna che nella vena Azygos (fig.7).
Questa risposta neurologica favorevole è stata pure confermata dalla significativa riduzione delle lesioni gadolino positive alla RM perfusionale a distanza di un anno; risultato importante perchè
ottenuto in cieco.
Tuttavia il nostro progetto open label richiede una certa prudenza nel dare un peso a questo dato.
La RM perfusionale non è stata sempre eseguita con lo stesso strumento o seguendo lo stesso protocollo, nè agli stessi intervalli di tempo.
Questo aspetto discutibile è collegato con il disegno open-label del nostro studio, cosi come col dato non trascurabile che abbiamo trattato i nostri pazienti al momento stesso della verifica diagnostica con flebografia della presenza della stenosi.
Un altro fattore importante per spiegare l’esito favorevole ottenuto nel gruppo di pazienti a decorso RR potrebbe essere il trattamento continuativo immuno-modulato, che com’è noto è da solo in grado
di ridurre in modo significativo le lesioni Gad pos rilevabili alla RM perfusionale35,36
Tuttavia l’evidenza assoluta che si evince dal nostro studio è che il trattamento endovascolare della CCVSI è in grado di determinare un ulteriore beneficio alle lesioni della SM.
I risultati neurologici nei gruppi progressivi primari e secondari sono stati sicuramente meno significativi e promettenti.
Comunque, dato che il decorso PP è orfana di qualsiasi trattamento effettivo, il miglioramento significativo della Qqo fisica, ci suggerisce ulteriori valutazioni su un campione più grande di pazienti PP.
Sarà interessante conoscere, quando disponibile, la valutazione della pervietà secondaria nel gruppo di 30 pazienti che si sono sottoposti a PTA una seconda volta per le restenosi nella vena
giugulare interna.
Il difetto principale del nostro studio è rappresentata dal fatto di non essere uno studio “cieco”, per cui esiste una grande possibilità che tale difetto possa ingenerare una speranza nel trattamento di questa patologia neurologica associata a CCSVI.
Comunque questi dati sono preziosissimi da un punto di vista scientifico per progettare uno studio di controllo multicentrico e randomizzato con osservatori “ciechi” dell’esito neurologico.
Tale studio dovrebbe confrontare due gruppi di pazienti a decorso RR, l’uno trattato solo farmacologicamente e l’altro in cui il trattamento endovascolare della CCVSI viene associato al
trattamento farmacologico della SM.
Bibliografia
1. Schaller B (2004) Physiology of cerebral venous blood flow:
from experimental data in animals to normal function in humans.
Brain Research Reviews 46:243– 260
2. Menegatti E, Zamboni P (2008) Doppler haemodynamics of
cerebral venous return. Curr Neurovasc Res 5:260-5.
3. Lepori D, Capasso P, Fournier D, Genton CY, Schnyder P.:
High-resolution ultrasound evaluation of internal jugular venous
valves. Eur Radiol.1999;9:1222-6
4. Zamboni P, Galeotti R, Menegatti E, Malagoni AM, Tacconi G,
Dall’Ara S, et al. Chronic Cerebrospinal Venous Insufficiency In
Patients With Multiple Sclerosis. J Neur Neurosurg Psychiatry
2009;80:392-9
5. Lee BB, Laredo J, Lee TS, Huh S, Neville R. Terminology and
classification of congenital vascular malformations. Phlebology.
2007;22:249-52.
6. Zamboni P, Menegatti E, Galeotti R, Malagoni AM, Tacconi G,
Dall'ara S, et al. The value of cerebral Doppler venous
haemodynamics in the assessment of multiple sclerosis. J Neurol
Sci. 2009 15;282:21-7.
7. Franceschi C. The unsolved puzzle of multiple sclerosis and
venous function. J Neurol Neurosurg Psychiatry. 2009;80:358.
8. Zamboni P, Consorti G, Galeotti R, Gianesini S, Menegatti E,
Tacconi G, et al. Venous Collateral Circulation Of The Extracranial
Cerebrospinal Outflow Routes. Curr Neurovasc Res 2009 Aug 1.
[Epub ahead of print]
9. Law M, Saindane AM, Ge Y, James SB, Glyn J, Lois JM,
Joseph H, Robert IG. Microvascular abnormality in relapsingremitting multiple sclerosis: perfusion MR imaging findings in
normal-appearing white matter. Radiology 2004;231:645–52.
10. Ge Y, Zohrabian VM, Grossman RI, Seven-Tesla Magnetic
Resonance Imaging. New Vision of Microvascular Abnormalities in
Multiple Sclerosis. Arch Neurol 2008;65:812-816.
11. Kermode AG, Thompson AJ, Tofts P, MacManus DG, Kendall
BE, Kingsley DP, et al. Breakdown of the blood-brain barrier
precedes symptoms and other MRI signs of new lesions in multiple
sclerosis. Pathogenetic and clinical implications. Brain
1990;113:1477-89.
12. Kidd D, Barkhof F, McConnell R, Algra PR, Allen IV, Revesz T.
Cortical lesions in multiple sclerosis. Brain 1999;122:17-26
13. Tan IL, van Schijndel RA, Pouwels PJ. MR venography of
multiple sclerosis. Am J Neuroradiol 2000;21:1039-42.
14. Fog T. The topography of plaques in multiple sclerosis with
special reference to cerebral plaques. Acta Neurol Scand Suppl
1965;15:1-161.
15. Noseworthy JH, Lucchinetti C, Rodriguez M, Weinshenker BG.
Multiple sclerosis. N Engl J Med. 2000;343:938-52.
16. Polman CH, Reingold SC, Edan G, Filippi M, Hartung H-P.
Diagnostic Criteria for Multiple Sclerosis: 2005 Revisions to the
ìMcDonald Criteriaî Ann Neurol 2005;58:840-846
17. Kurtzke JF. Rating neurological impairment in multiple
sclerosis: an expanded disability scale (EDSS). Neurology
1983;33:1444-52.
18. Lee BB, Villavicencio L, Kim YW, Do YS, Koh KC, Lim HK, et
al. Primary Budd-Chiari syndrome: outcome of endovascular
management for suprahepatic venous obstruction. J Vasc Surg.
2006 ;43:101-8.
19. Raju, S; Hollis, K; Neglen, P. Obstructive lesions of the inferior
vena cava: clinical features and endovenous treatment. J Vasc
Surg 2006; 44: 820.
20. Viscusi ER, Reynolds L, Chung F, Atkinson LE, Khanna S.
Patient-controlled transdermal fentanyl hydrochloride vs
intravenous morphine pump for postoperative pain: a randomized
controlled trial. JAMA. 2004;17:1333-41.
21. Cutter GR, Baier ML, Rudick RA, Cookfair DL, Fischer JS,
Petkau J. et al. Development of a multiple sclerosis functional
composite as a clinical trial outcome measure. Brain
1999;122:871-82.
22. Fisher JS, Rudick R, Cutter G, Reingold SC. The Multiple
Sclerosis Functional Composite measure (MSFC): an integrated
approach to MS clinical outcome assessment. Mult Scler
1999;5:244-50.23. D'Souza M, Kappos L, Czaplinski A. Reconsidering clinical
outcomes in Multiple Sclerosis: relapses, impairment, disability and
beyond. J Neurol Sci. 2008;274:76-9.
24. Weinstock-Guttman B, Ramanathan M, Zivadinov R.
Interferon-beta treatment for relapsing multiple sclerosis. Expert
Opin Biol Ther. 2008;8:1435-47.
25. Freedman MS, Hughes B, Mikol DD, Bennett R, Cuffel B,
Divan V, et al. Efficacy of disease-modifying therapies in relapsing
remitting multiple sclerosis: a systematic comparison. Eur Neurol.
2008;60:1-11.
26. Vickrey BG, Hays RD, Harooni R, Myers LW, Ellison GW. A
health-related quality of life measure for multiple sclerosis. Qual
Life Res. 1995;4:187-206.
27. Geerts WH, Bergqvist D, Pineo GF, Heit JA, Samama CM,
Lassen MR, et al; American College of Chest Physicians.
Prevention of venous thromboembolism: American College of
Chest Physicians Evidence-Based Clinical Practice Guidelines (8th
Edition). Chest. 2008;133(6 Suppl):381S-453S.
28. Zamboni P, Lanzara S, Mascoli F, Caggiati A, Liboni A.
Inflammation in venous disease. Int Angiol. 2008;27:361-9.
29. Zamboni P. The big idea: iron-dependent inflammation in
venous disease and proposed parallels in multiple sclerosis. J R
Soc Med. 2006;99:589-93.
30. Schelling, F. Damaging venous reflux into the skull or spine:
relevance to multiple sclerosis. Med Hypotheses 1986;21:141-148.
31. Talbert DG. Raised venous pressure as a factor in multiple
sclerosis Med Hypotheses 2008;70:1112-7.
32. West JB, Tsukimoto K, Matheu-Costello O, Prediletto R Stress
failure in pulmonary capillaries. J Appl Physiol1991;70:1731–42.
33. Browse NL, Burnand KG. The cause of venous
ulceration.Lancet. 1982;2:243-5
34. Xu K, He FX, Zhang HG, Zhang XT, Han MJ, Wang CR, et al.
Budd-Chiari syndrome caused by obstruction of the hepatic inferior
vena cava: immediate and 2- year treatment results of transluminal
angioplasty and metallic stent placement. Cardiovasc Intervent
Radiol. 1996;19:32-6.
35. Havrdova E, Galetta S, Hutchinson M, Stefoski D, Bates D,
Polman CH, et al. Effect of natalizumab on clinical and radiological
disease activity in multiple sclerosis: a retrospective analysis of the
Natalizumab Safety and Efficacy in Relapsing-Remitting Multiple
Sclerosis (AFFIRM) study. Lancet Neurol. 2009;8:254-60.
36. CAMMS223 Trial Investigators, Coles AJ, Compston DA,
Selmaj KW, Lake SL, Moran S, et al. Alemtuzumab vs. interferon
beta-1a in early multiple sclerosis. N Engl J Med. 2008;359:1786-
801.
PUBBLICAZIONI VECCHIE DELLA - Fondazione Hilarescere ONLUS 2008











.jpg)
.jpg)
.jpg)














.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)














