low-dose-naltrexone.de/
SITO LDN NORVEGIA
http://www.ldn/
SITO RACCOLTA TESTIMONIANZE LDN
www.ldndatabase.com
SITO RICERCHE LDN INGLESE
http://
www.ldnresearchtrust.org/
default.asp?page_id=77
SITO LDN INGLESE
http://www.ldnaware.org/
Per quali patologie e'utilizzato e che risultati si hanno
>Il dott. Bernard Bihari,e anche altri medici e ricercatori hanno
stabilito che ldn puo' essere d'aiuto in diverse patologie.
**
Tumori Altre patologie
tumore alla vescica
tumore al seno
Carcinoma
tumore al colon e retto
Glioblastoma
tumore al fegato
tumore al polmone(non a cellule piccole)
leucemia linfocitaria
Linfoma (Hodgkin's e Non-Hodgkin's)
Melanoma maligno
Mieloma multiplo
Neuroblastoma
tumore alle ovaie
tumore al pancreas
tumore alla prostata(inoperabile)
carcinoma ai reni
tumore alla gola
tumore dell'utero
SLA (malatt.di Lou Gehrig o scl.lat.amiotr.) ***
SLP (sclerosi laterale primaria-pls in inglese)***
Alzheimer ********
Spondillite anchilosante
Autismo ************
malattia di Behcet
Celiachia
Sindrome da fatica cronica
sindrome di CREST
morbo di Crohn
Emphysema (COPD)
Endometriosi
Fibromyalgia
Sindrome di Sjogren
HIV/AIDS
sindrome dell'intestino irritabile (IBS)
Sindrome di Sjogren
Sclerosi multipla (SM)**********
Parkinson **********
Sclerosi laterale primaria (PLS)
Psoriasis
Artrite reumatoide
Sarcoidosi
Sclerodermia
Sindrome di Stiff Person (SPS)
Lupus Sistemico(SLE)
Mielite trasversa
Colite ulcerativa
Granulomatosi di Wagner
CSS sindrome diChurg Strauss
> LDN si e' dimostrato efficace in centinaia di casi
CANCRO:come dallo stesso riportato, a meta'del 2004 il Dott.Bihari
aveva trattato piu'di 300 pazienti che erano affetti da un tumore che
avevano dato esito negativo al trattamento con le terapie standard
antitumorali. Di quel gruppo circa il 50% in trattamento con ldn dopo
4-5 mesi ha cominciato a mostrare segni di stop alla crescita del tumore
e di quelli i due terzi hanno mostrato un obiettivo restringimento del
tumore
MALATTIE AUTOIMMUNI :dei pazienti in cura per
una malattia autoimmune(vedi elenco sopra)nessuno ha fallito nel
dimostrare di rispondere alla terapia con LDN,tutti hanno mostrato uno
stop della progressione della loro malattia. In molti pazienti c'e'
stata una marcata remissione dei sintomi e dei segni della patologia
.Il maggior numero di pazienti con malattie autoimmuni erano persone
con sclerosi multipla. Di questi circa 400 erano in cura diretta dal
dr.Bihari. Meno dell'1%di questi pazienti ha manifestato un nuovo
attacco o ricaduta dovuta alla sm mentre mantenevano regolarmente la
terapia con LDN assunto ogni sera prima di dormire.
.
HIV/AIDS:A settembre del 2003 il dr Bihari stava trattando con LDN 350
pazienti afffetti da AIDS in contemporanea con le terapie anti aids
ufficiali. Passati i primi 7 anni piu' del 85% di questi pazienti non
mostrava livelli rilevabili di virus HIV,un successo molto maggiore
delle normali terapie in uso per AIDS,e tutto senza significativi
effetti collaterali. E anche una nota importante il fatto che molti
pazienti sono stati senza sintomi della malattia per anni assumendo solo
LDN e nessuna altra medicina.
DISORDINI DEL SISTEMA
NERVOSO CENTRALE:rilevazioni e osservazioni anedottiche hanno
confermato i benefici dell'uso di ldn in malattie come
Alzheimer,Parkinson,Sla, e sclerosi laterale primaria. Inoltre la dott.
Jaqueline Mcandless ha scoperto un effetto molto positivo di LDN in
forma appropriatamente ridotta e applicato come crema nei bambini con
autismo.
.
> Come e' possibile che un farmaco possa avere effetto su cosi'tante e diverse patologie.
Le patologie elencate sopra hanno tutte un fattore comune:in tutte loro
il sistema immunitario gioca un ruolo fondamentale.Un basso livello di
endorfine nel sangue generalmente sempre associato a immunodeficienza
contribuiscono a sviluppare la patologia
Altri ricercatori
lavorando sui recettori neuropeptidi presenti in diversi tumori umani,
hanno trovato recettori oppioidi in diversi tipi di tumore:
Tumore al cervello (entrambi astrocitoma e glioblastoma)
Tumore al seno
Tumore endometriale
Carcinoma a cellule squamose di testa e collo
Leucemia mieloide
Tumore al polmone(entrambi con cellule piccole e cell.non piccole)
Neuroblastoma e altri...
Questa scoperta suggerisce che e' possibile beneficiare di LDN in una vasta quantita' di tumori
Che dosaggio e frequenza d'assunzione il mio medico mi deve prescrivere?
La dose abituale per adulti e' di 4,5 mg /die presa di sera prima di
addormentarsi,questo per via del ritmo corporeo di produzione degli
ormoni principali. E'meglio prendere LDN tra le 21,00 e le0300 .i piu'
tanti lo assumono prima di andare a dormire
Eccezioni da considerare:
Persone con la sclerosi multipla che sono soggetti a rigidita' e
spasmi alle gambe sono avvisati di iniziare gradualmente prima di
arrivare alla dose di 3 mg,e quindi di non superare mai quella dose
Per definire il dosaggio iniziale di LDN in quei pazienti affetti da
tiroidite di Ashimoto con ipotiroidismo e che stanno assumendo farmaci
per riequilibrare gli ormoni della tiroide e' bene consultare le
avvertenze e precauzioni riportate sotto.
Se viene utilizzato
il naltrexone cloridrato liquido(antaxone) ottenuto dalle confezioni di
boccette da 50mg vendute in farmacia e prodotte dalla ditta Zambon,
considerando che un flaconcino da 50 mg dura oltre 12 giorni lo stesso
dopo l'apertura tra un uso e l'altro va chiuso e tenuto in frigorifero
Il range terapeutico della dose di LDN va da 1,7 mg a 4,5 mg presi ogni
notte prima di coricarsi(dopo le 2100 e non oltre le 0300)a dosi
inferiori si suppone che LDN non abbia effetti, mentre dosaggi superiori
si ritiene che blocchino le endorfine per un tempo troppo lungo,questo
interferisce con la sua efficacia
Ci sono effetti collaterali o precauzioni da prendere?
> Effetti collaterali:
LDN non ha virtualmente nessun effetto collaterale.
Occasionalmente,durante le prime settimane di assunzione i pazienti
possono lamentare alcune difficolta' nell'addormentarsi. Questo
raramente perdura dopo le prime settimane. Dovesse perdurare allora il
dosaggio puo' essere ridotto da 4.5 a 3 mg per notte.
> Avvertenze e precauzioni
Siccome LDN blocca i recettori degli oppioidi attraverso il corpo
per 3-4 ore,persone che stanno assumendo medicine che sono agonisti
degli oppioidi o medicine su base narcotica come ad es Ultram
(tramadol),morfina,Percoce
t,Duragesic
o farmaci conteneti codeina ,queste non devono assumere LDN fino a
quando tali farmaci non saranno completamente fuori dall'organismo.
Pazienti che per assunzione di medicine su base narcotica ne sono
diventati dipendenti devono aspettare 10-20 giorni dall'interruzione di
tali farmaci all'inizio di LDN
Quei pazienti che stanno
assumendo farmaci per il ripristino dei valori degli ormoni della
tiroide in caso ad esempio di diagnosi di tiroidite di Ashimoto e hanno
ipotiroidismo dovranno iniziare LDN al dosaggio minimo di 1,5
mg(adulti)Fate attenzione che LDN potrebbe originare una pronta
riduzione dell'attivita' della malattia autoimmune che richiederebbe una
rapida riduzione nella dose dei farmaci che aumentano gli ormoni della
tiroide,in modo da evitare i sintomi di un ipertiroidismo .
La
dose piena di naltrexone, ha parecchie controindicazioni e avvertenze
per l'uso in pazienti con disordini al fegato.Queste avvertenze furono
istituite per via degli effetti collaterali al fegato rilevati in
esperimenti coinvolgenti pazienti che assumevano 300 mg/die La dose di
50 mg/die non provoca apparentemente alterazioni dei valori del fegato e
naturalmente e' ancora piu' sicura una dose molto piu' ridotta di soli
3-4,5 mg/die
Persone che hanno subito il trapianto di un organo
e che stanno utilizzando farmaci immunosopressori,devono evitare di
assumere ldn.
COME POSSO OTTENERE LDN
LDN puo'essere prescritto oltre che dal
neurologo dal proprio medico curante ed essere preparato
da una farmacia specializzata in preparazioni galeniche
Il naltrexone necessita di ricetta medica
pertanto il medico deve rilasciare ricetta nel momento che viene
deciso di utilizzare tale trattamento
Il naltrexone in dose maggiore di 50 mg e' stato in origine
prodotto da Du Pont negli Stai Uniti con il nome
commerciale di ReVia. In Italia un prodotto simile ha il nome
commerciale di Antaxone ed e' prodotto dalla Zambon(antaxone e'
naltrexone cloridrato)
IMPORTANTISSIMO:
assicuratevi di specificare al
farmacista che realizza la preparazione che non si vuole assolutamente un
prodotto a formula di rilascio lento o sr(slow relise)
Verifiche fatte sull'osservazione dei pazienti
hanno evidenziato che un rilascio non immediato di ldn
nell'organismo inibisce l'azione dello stesso rendendone vana
l'efficacia
Importantissimi sono anche gli eccipienti usati per produrre
la capsula(filler),l'esperienza della farmacia del dott.Skip
Lenz ha evidenziano che non deve assolutamente essere utilizzato
carbonato di calcio,in quanto interferisce con l'assorbimento di
LDN da parte dell'organismo
Viene raccomandato dal dott.Skip di utilizzare cellulosa
microcristallina o avicel,lattosio(se non si e' intolleranti al
lattosio) o eccipienti a base di saccarosio sempre in confezione
a rilascio immediato
IMPORTANTE:assicurarsi di
rivolgersi ad una farmacia che abbia una buona esperienza
nelle preparazioni galeniche.
Il dott.Bihari ha rilevato che
l'assunzione di capsule di naltrexone a basso dosaggio
preparate da farmacie poco esperte nelle preparazioni
galeniche di LDN erano la causa di molti fenomeni
avversi
DOSE CON FLACONCINI DELLA FARMACIA PIAZZAVILLARI
I flaconcini di sciroppo i ldn prodotti
dalla farmacia Piazzavillari sono composti da:naltrexone
50 mg, sorbitolo 70%, metile p-ossibenzoato, propile
p-ossibenzoato, acqua depurata il tutto in un in
flaconcino da 20 ml.Questo chiaramente significa che la
concentrazione e' la meta'di quella di antaxone,pertanto la
stessa procedura con la siringa da insulina sara' fatta
considerando di aspirare il doppio della dose che si aspira
con antaxone.(1 tacca corrisponde a 0,25 mg pertanto 1 mg
corrisponde a 4 tacche)
1^sett. 8 tacche della siringa=2 mg
2^sett.10tacche della siringa=2.5 mg.
3^sett.12 tacche della siringa(2volte
6 tacche)=3 mg.
10^ sett.14 tacche della siringa(2
volte 7 tacche)=3,5 mg
15^ sett.16 tacche della siringa(2
volte 8 tacche)=4 mg.
25^ sett.18 tacche della siringa(2
volte 9 tacche)=4,5 mg.
Per il resto le modalita' sono le stesse,spruzzare in bocca e non
iniettare,riporre in frigorifero chiuso il flaconcino una volta aperto.
COME PREPARARE LA DOSE CON ANTAXONE
Bottiglino da 50 mg di naltrexone(10 ml.) e
siringa da insulina 1 ml.(10 tacche da 0.1 ml)
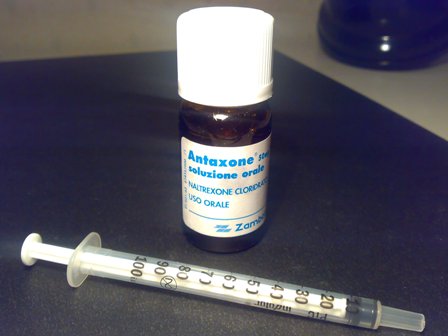
Per procedere alla preparazione della dose detta :
fatta in casa,ci si deve procurare i flaconcini di antaxone liquido
commercializzati dalla ditta Zambon e reperibili con ricetta medica in qualsiasi
farmacia. La confezione contiene 10 flaconcini da 10 ml (50 mg.) di naltrexone
cloridrato liquido. Occorre quindi disporre di un dispositivo in grado di calibrare
la quantita' di naltrexone da prelevare dal flaconcino. E' pratica sicura e facile
da realizzare quella utilizzando una siringa da insulina da 1 ml graduata in 10
tacche da 0.1 ml cadauna. Siccome la soluzione contenuta nel flaconcino e' al
5%(10ml corrispondono a 50 mg) e siccome una tacca della siringa
corrisponde a 0.1 ml=0.5 mg, se ne deduce che per avere la dose iniziale di 2 mg
occorre aspirare 4 tacche dal flacone. Si procede quindi di sett. in sett. all' aumento
graduale di una tacca fino ad arrivare alla dose max. di 9 tacche =4,5 mg. Di
seguito riportiamo una tabella riassuntiva consigliata:
1^sett. 4 tacche della siringa=2 mg.
2^sett.5tacche della siringa=2.5 mg.
3^sett.6 tacche della siringa=3 mg.
10^ sett.7 tacche della siringa=3,5 mg
15^ sett.8 tacche della siringa=4 mg.
25^ sett.9 tacche della siringa=4,5 mg.
Il naltrexone deve essere spruzzato in bocca (non
iniettato)
quindi per maggior sicurezza una volta aspirato e' bene rimuovere l'ago
dalla siringa. un flacone da 50 mg.(10ml) dura quindi per un periodo di
11 giorni a dose
piena,per periodi superiori se la dose utilizzata e' inferiore. va
quindi una
volta aperto,richiuso e conservato in frigorifero .chiaramente la dose
indicata
dal dott.bihari di 4,5 mg e' la dose max. in modo da non ottenere
risultato
contrario,e'la dose che lui riteneva fondamentale e che tutti dovrebbero
cercare
di raggiungere. nella sm per i problemi di rigidita' e spasticita' viene
consigliato a chi incorre in questi problemi e ne rileva l'aumento con
l'assunzione di ldn, di non superare i 3 mg. sondaggi effettuati tra
tutti gli
utilizzatori di ldn sparsi per il mondo hanno accertato che anche a dosi
minori(non inferiori comunque a 2 mg.) ldn funziona senza dare i
problemi
precedentemente descritti
ALTRI PRODOTTI REPERIBILI IN ITALIA EQUIVALENTI AD ANTAXONE SONO NARCORAL
E NALOREX,ENTRAMBI SONO "NALTREXONE CLORIDATO". LA PROCEDURA E' UGUALE A QUELLA PER ANTAXONE .
IMPORTANTE
L'ORARIO D'ASSUNZIONE VA DALLE 21,30 ALLE 03,00
DEL MATTINO BISOGNA TENERE IN CONSIDERAZIONE IL FATTORE ORA LEGALE DEL PERIODO
ESTIVO,INFATTI QUANDO SI SPOSTA L'OROLOGIO UN'ORA AVANTI PER
GUADAGNARE IN LUCE SOLARE AUTOMATICAMENTE SI
DEVE RITARDARE L'ASSUNZIONE ALLE ORE 22,30
NEWS
- FARMACIA CAIROLI (Tutti i preparati galenici)
Del Dr. Buglioni FabrizioCorso Cairoli, 18
62100 Macerata
Tel.: 0733 232760
fax 0733 267035
Indirizzo e-mail: farmaciacairoli@virgilio.it
(sconto in base alla quantità di capsule richieste)
NEWS
Pesaro-Urbino
(PU):
Farmacia Casinina Dr. Orazi Fabio
Via Provinciale45
61020 Auditore PU
Tel e Fax 0722-362512
e_mail casinina@farmacieufi.it
 Sanita': allarme diabete infantile, a Napoli 'I salotti di Sanofi'
Sanita': allarme diabete infantile, a Napoli 'I salotti di Sanofi'
 www.cannabis-med.org/index.php?lng=it&fb_source=message
www.cannabis-med.org/index.php?lng=it&fb_source=message
